质量风险管理制度
VIP免费
######### 有限公司
文件编号 质 量 风 险 管 理 制 度 版本/替代
##-SOP-××× 00/
颁发部门:质量部 起 草: 审 阅:
审 核: 批准人: 执行日期:
分发部门:
1 目 的
建立质量风险管理制度,规范药品生命周期中质量风险的评估、控制与审核操作行为,降低产
品的质量风险。
2适用范围
适用于公司所生产药品其质量风险的评估、控制与审核的管理
3术语或定义
质量风险:是一个系统化的过程,是对产品在整个生命周期过程中,对风险的识别、衡量、控
制以及评价的过程。质量风险管理:是对药品整个生命周期进行质量风险的识别、评估、控
制、沟通、回顾的系统过程,运用时可采用前瞻或回顾的方式。
4 职 责
质量部:负责组织进行质量风险评估、控制与审核协调、管理等相关事宜。
职能部门:对本规程的实施负责。
5安全注意事
项 不适用于
本文
6 规 程
6.1风险管理的内容
6.1.1风险管理包括的内容有风险评估、风险控制、风险沟通和审核等程序,持续地贯穿
于整个产品生命周期。
6.1.2风险评估是风险管理过程的第一步,它包括风险识别,风险分析和风险评价三个部
分 即解决三个基本问题:(1将会出现的问题是什么?(2可能性有多大?(3 生的后问题发
果是 什么?
6.1.3风险控制的目的就是将风险降低到可接受的水平。重点归纳为:(1)风险是否在可以
被接受的水平上?(2)可以采取什么 的措施来降低、控制或消除样 风险?(3)在控制已经识别
的 是否会 生新的风险时 产 风险?
6.1.4风险沟通:通过风险沟通,能够促进风险管理的实施,使各方掌握更全面的信息从
而调整或改进措施及其效果。
6.1.5风险审核:在风险管理流程的最后阶段,应该对风险管理程序的结果进行审核,尤
其是对那些可能会影响到原先质量管理决策的事件进行审核。
6.2风险管理程序
6.2.1风险管理的启动
6.2.1.1确定问题和/或有关风险的疑问,包括确认风险可能性的相关假设;
6.2.1.2风险管理小组负责召集与风险相关的部门或专家,收集与所评估的风险相关的可
能性危 、危害或 人体健康的影响的有关背景 料和数据。险 对 资
6.2.1.3根据存在的主要风险的性质确定风险管理的组长和必要的资源。
6.2.1.4确定如何使用这些信息,评估和结论;
第 4 页 / 共 4 页
######### 有限公司
文件编号 质 量 风 险 管 理 制 度 版本/替代
##-SOP-××× 00/
颁发部门:质量部 起 草: 审 阅:
审 核: 批准人: 执行日期:
分发部门:
6.2.1.5根据具体的问题,由风险管理的组长负责组织建立风险管理流程,包括详细的时
间计划。
6.2.2风险评估:首先系统地利用各种信息和 来确 工 、 、系 、操作等 程经验 认 艺 设备 统 过
中存在的风险,指出将会出现的问题在哪里。包括识别可能的后果,为进一步质量风险管
理进程的其它步骤提供基础;其次对已经被识别的风险及其问题进行分析, 需要相当有这
经验的技术人员以及QA 相关人员共同完成,通过分析确认将会出现问题的可能性有多大,
出现的问题是否能够被及时地发现以及造成的后果等,然后并参照预先确定的风险标准对
风险进行评价(可以 的等 表示风险 级 );最后讨论风险问题的危害会引起其它什么 ,问题
后果会是什么?得出定量的结论:即使用从0%~100%的可能性数 来表示。另外,也值
可 “ ” “ ” “ ”以对风险进行定性描述,比如高、 中 、 低 。
6.2.3风险控制包括作出决策来降低和/或接受风险。风险降低针对风险评估中确定的风险
进行改进,通过实施一些措施使风险降低。接受风险是指考虑到风险等级和降低风险所需
的成本两个方面,从而 定一个可以接受的 等 , 一旦 降低至 等 ,就接受设 风险 级 风险 该 级 该
风险而不用再采取更严格的措施进一步降低风险。
6.2.4风险沟通:在风险控制与最后的风险回顾(风险审核)中间一般会包括一个风险交
流的步骤,是指在采取了风险控制措施以后,需要通过实际的生产或操作来检查上述风险
控制的措施是否有效,是否可以将风险降低至预期的等级。在风险管理程序实施的各个阶
段,决策者和相关部门应该对进行的程度和管理方面的信息进行交换和共享,通过风险沟
通,能够促进风险管理的实施,使各方掌握更全面的信息从而调整或改进措施及其效果。
6.2.5风险审核:是指通过一段时间的运行,需要对整个系统的风险进行审核,因为之前采
用的风险控制措施也许没有效果,也或许工艺或设备等发生了一些变更,从而需要对整个
过程进行再评估,甚至如果变更是个很重大的变更,应该在变更执行完以后就立刻开始风
险回顾的工作。风险管理是一个持续性的质量管理程序,应当建立阶段性审核检查的机制,
审核频率应当建立在相应的风险水平之上。
6.3常用的风险管理工具
6.3.1通常用组织数据和简化决策用图表形式:流程图、检查表、控制图、因果图
6.3.2非正式工具一以经验和企业内部 SOP 为基础,被实践证明行之有效:质量审计、
投 诉处理、产品质量趋势分析、偏差处理, CAPA 等
6.3.3正式管理工具一在足够数量的基础数据支持下,可定量或半定量地进行风险管理
缺陷模式效应分析:通过分析生产过程的各种潜在缺陷模式以判断其对产品可能的后果;
降低风险的方法针对各种缺陷模式;通过解析生产过程,将复杂问题简单化;将缺陷、缺
陷的原因和缺陷的后果联系起来
6.7风险管理的实际运用
6.7.1作为质量管理体系一部分的质量风险管理
6.7.1. 文件: 核法 方面最新的 和 用,确定开 新的审 规 释义 应 发 SOP 的需求,指南。
6.7.1.教育与培训:员工素质的基础教育、经验的传授和工作习惯的形成,以及对前阶
段培训的定期评价(或效果 )。
6.7.1. 质量缺陷:为识别、评估和沟通可疑的质量缺陷、投诉、趋势、偏差、调查和OOS
第 4 页/共4页
######### 有限公司
文件编号 质 量 风 险 管 理 制 度 版本/替代
##-SOP-××× 00/
颁发部门:质量部 起 草: 审 阅:
审 核: 批准人: 执行日期:
分发部门:
结果等对产品质量的潜在影响提供基础。促进与药品管理机构之间的风险沟通及确定
解 决严重的质量缺陷的适宜措施(如,产品召回)
6.7.1.审计/检查:在确定审计的范围和频率时,不论是内部的还是外部的,应考虑以下
因素:现行的法规要求、企业总体符合规范的状况和历史、场地的复杂性、生产工艺的
复杂性、药品本身特性的复杂性、质量缺陷的数量和严重性(如召会)、以前审计和检
查结果、各种变更、某产品的生产情况(如频率、周期、批量)等
6.7.1.周期性审核:选择、评估和解释产品质量评审所得数据的趋势结果、解释监控数
据(如,对再验证需求的评价、取样方面的变更)
6.7.1.6变更管理/变更控制:基于药品开发和生产过程中积累的知识和资料来管理变更。
评估变更对最终产品的可获得性的影响。评估厂房、设备、物料、制造工艺或技术转移
的变更对产品质量的影响。在实施变更前确定应采取的适宜行动,如,附加测试,(再)
确认,(再)验证,与管理机构沟通。
6.7.1.作为开发的一部分的质量风险管理:选择最佳的产品设计(如胃肠外浓缩液对预
混)和工艺设计(如,制造工艺、终端灭菌对无菌工艺)、加强不同的物料性质(如,
粒径分布、水分控制、流动性能)、不同的加工方式和工艺参数对产品性能的影响的了
解、 估原料、溶 、活性成分评剂 (API) 的起始物料、活性成分、辅料或包装材料的关
键 属性、建立适宜的规格标准与生产控制要求(如,如,运用药品开发研究中来自对质
量 属性在临床上的重要性和在生产过程中控制的可能性方面考虑的信息)、以减少质
量属 性的变化(如:减少物料和产品缺陷、减少生产缺陷、减少人为差错)、评价与放
大和 技术转移相关的附加研究需求(如,生物等效性,稳定性)
6.7.2厂房、设备、设施的质量风险管理
6.7.2.厂房、设备的设计:当设计建筑物核厂房时应确定适宜的区域(如,物料和人的
流向、将污染降至最低、有害生物控制措施、防止混淆、开放与密闭设备、洁净室与隔
离器技术、专用或隔离的厂房/设备)、为设备和容器确定适宜的产品接触材料、确定适
宜的辅助设施、对相关设备确定适宜的预防性维护。
6.7.2.2房的卫生方面:保护产品免受周围环境的危害,包括化学的、微生物的、物理
的危害、保护环境(如,人员、潜在的交叉污染)免受与所生产的产品相关的危害
6.7.2.3房、设备、设施的确认:确定厂房、建筑、生产设备和/或实验仪器的确认范围
和程度,包括适宜的校正方法。
6.7.2.设备清洁和环境控制:根据使用意图确定努力和决定的差异(如,多重目的对单
一目的、单批对连续性生产)、确定可接受的清洁验证限度
6.7.2.胶正/预防性维护:设定适宜的校正与维护时间表
6.7.2.6十算机系统和计算机控制的设备:选择计算机硬件和软件的设计(如,模块、架
构、容错)、确定验证范围(如,关键性能参数的识别、要求与设计的选择、代码审查、
测试的范围与测试方法、电子记录和签名的可靠性)
6.7.3作为物料管理一部分的质量风险管理
6.7.3.供应商和委托制造商的评价与评估:对供应商和委托制造商提供综合性的评
估(如,审计、供应商质量协议)
第 4 页 / 共 4 页
摘要:
展开>>
收起<<
#########有限公司文件编号质量风险管理制度版本/替代##-SOP-×××00/颁发部门:质量部起草:审阅:审核:批准人:执行日期:分发部门:1目的建立质量风险管理制度,规范药品生命周期中质量风险的评估、控制与审核操作行为,降低产品的质量风险。2适用范围适用于公司所生产药品其质量风险的评估、控制与审核的管理3术语或定义质量风险:是一个系统化的过程,是对产品在整个生命周期过程中,对风险的识别、衡量、控制以及评价的过程。质量风险管理:是对药品整个生命周期进行质量风险的识别、评估、控制、沟通、回顾的系统过程,运用时可采用前瞻或回顾的方式。4职责质量部:负责组织进行质量风险评估、控制与审核协调、...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
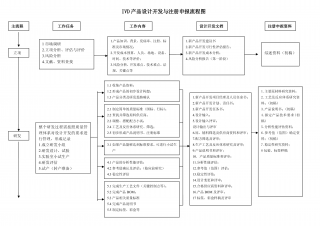
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者:冒牌货
分类:实用文档
价格:50质量币
属性:4 页
大小:43.5KB
格式:DOC
时间:2026-01-07


