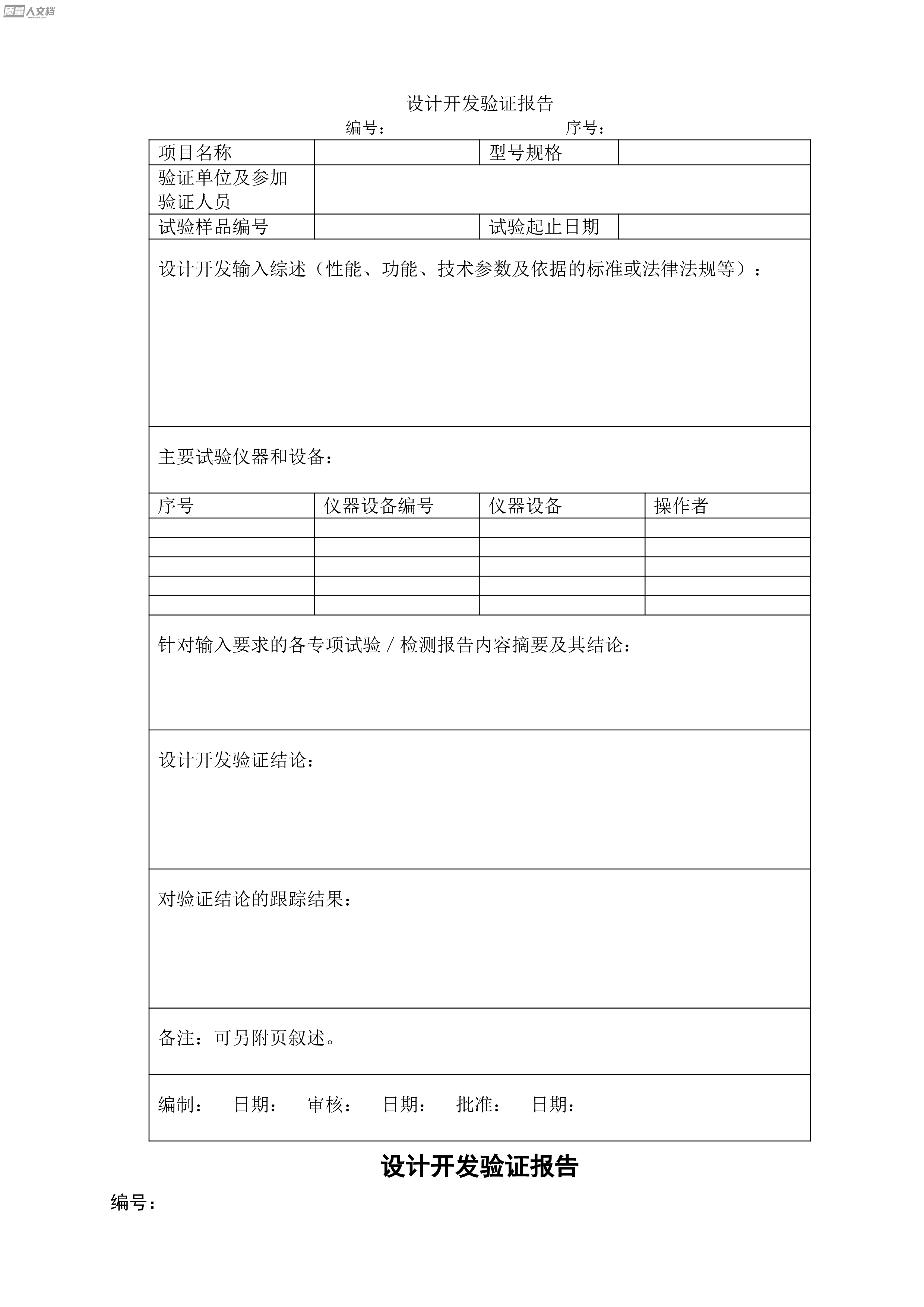
设计开发验证报告


摘要:
展开>>
收起<<
设计开发验证报告编号:序号:项目名称型号规格验证单位及参加验证人员试验样品编号试验起止日期设计开发输入综述(性能、功能、技术参数及依据的标准或法律法规等):主要试验仪器和设备:序号仪器设备编号仪器设备操作者针对输入要求的各专项试验/检测报告内容摘要及其结论:设计开发验证结论:对验证结论的跟踪结果:备注:可另附页叙述。编制:日期:审核:日期:批准:日期:设计开发验证报告编号:项目名称验证方式参加验证部门/人:验证日期验证内容:验证结论:改进措施及其跟踪验证:备注:验证结果作为附件予以保持。编制:审核:批准:设计和开发控制程序1.目的对设计和开发的全过程进行控制,确保新产品能满足顾客的需求和期望及...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
史上最全的鱼骨图模板
 2024-05-04 106
2024-05-04 106 -
鱼骨图PPT模板 (2)

 2024-05-04 89
2024-05-04 89 -
鱼骨图PPT模板

 2024-05-04 113
2024-05-04 113 -
鱼骨图模板

 2024-05-04 105
2024-05-04 105 -
PEMS开发生命周期(模板)VIP免费

 2024-11-06 474
2024-11-06 474 -
可用性工程报告 - 医疗器械CE认证技术文档VIP专免

 2024-11-11 303
2024-11-11 303 -
ISO14971医疗器械风险管理报告(标准模版+参考模板)VIP免费

 2025-07-22 186
2025-07-22 186 -
GB 9706.205-2020检验报告内容模板VIP免费
 2025-09-10 46
2025-09-10 46 -
医疗器械生产质量管理体系自查报告模板VIP免费

 2025-10-14 137
2025-10-14 137 -
TSG 08-2017与TSG 08-2026《特种设备使用管理规则》各条款对照表VIP免费

 2026-04-21 90
2026-04-21 90
作者:盛夏阳光
分类:实用文档
价格:50质量币
属性:5 页
大小:48KB
格式:DOC
时间:2024-05-22


