ISO-TR 10993-22-2017 医疗器械生物学评价--第22部分纳米材料指南(中文)
技术报告 ISO/TR
10993-22
第 一 版
2017-07
医疗器械生物学评价——
第22部分:
纳米材料指南
医疗器械生物学评价——第
22
部分:纳米材料
指南
参 考 编 号 ISO/TR
10993-22:2017(E)
C ISO 2017
ISO /TR 10993-22:2017(E)
目录 页
前言.................................................................................................................................................................................................................................................... V
介绍..............................................................................................................................................................................................................................................
vVi
1范围.....................................................................................................................................................................
1
2规范性参考文献...................................................................................................................................................................................................................
2
3术语和定义..........................................................................................................................................................................................................................
2
4一般原则............................................................................................................................................................. 5
4.1 一般性考虑...............................................................................................................................................................................................
5
4.2 纳米材料的生物学评价........................................................................................................................ 6
4.3 纳米材料的分类.................................................................................................................................... 6
4.4 纳米材料等效性.................................................................................................................................... 8
5纳米材料的表征...................................................................................................................................................................................................................
8
5.1 一般性考虑.............................................................................................................................................................................................. 8
5.2 表征参数与方法.................................................................................................................................. 10
5.3 参考文献的使用...................................................................................................................................................................................14
6样品制备........................................................................................................................................................... 15
6.1 一般性考虑.............................................................................................................................................................................................15
6.2 纳米结构材料的特殊考量..................................................................................................................15
6.3 纳米物体的特殊考虑..........................................................................................................................15
6.4 纳米材料的特性、储存与稳定性......................................................................................................17
6.5 原液和给药分散体化学成分描述 ............ ...................... 17
6.6 股票分散度的特征分析......................................................................................................................... 18
6.7 原液分散体制备给药溶液的表征.........................................................................................................18
6.8 剂量指标.................................................................................................................................................................................................... 19
6.9 其他注意事项...........................................................................................................................................................................................19
6.9.1 内毒素...................................................................................................................................................................................19
6.9.2 杀菌....................................................................................................................................................................................... 20
7医疗器械中纳米颗粒的释放....................................................................................................................................... 21
7.1 一般性考虑................................................................................................................................................................................................ 21
7.2 降解产物.................................................................................................................................................. 2
7.3 纳米物体的磨损释放............................................................................................................................22
7.4 原位加工.............................................................................................................................................. 22
8毒代动力学............................................................................................................................................................................................................................. 22
8.1 一般性考虑................................................................................................................................................................................................. 2
8.2 影响毒代动力学的因素.........................................................................................................................23
8.2.1 理化性质................................................................................................................................ 23
8.2.2 生物分子吸附.........................................................................................................................24
8.2.3 暴露途径.................................................................................................................................... 25
8.2.4 一服................................................................................................................................................................................. 25
8.2.5 物种和性别............................................................................................................................25
8.2.6 测量技术................................................................................................................................ 26
9毒理学评价.......................................................................................................................................................... 26
9.1 一般性考虑............................................................................................................................................................................................... 26
9.2 体外细胞毒性试验................................................................................................................................ 27
9.2.1 一般性考虑............................................................................................................................................................................ 27
9.2.2 纳米材料对检测方法的干扰考量......................................................................................... 28
9.2.3 相关剂量与剂量指标的考量................................................................................................................................................ 28
9.2.4 纳米物体动力学的思考......................................................................................................... 28
9.3 遗传毒性、致癌性和生殖毒性.............................................................................................................. 29
9.3.1 一般性考虑............................................................................................................................................................................ 29
9.3.2 体外遗传毒性试验................................................................................................................. 30
9.3.3 体内遗传毒性试验................................................................................................................. 31
◎ISO 2017-版权所有 iii
摘要:
展开>>
收起<<
技术报告ISO/TR10993-22第一版2017-07医疗器械生物学评价——第22部分:纳米材料指南医疗器械生物学评价——第22部分:纳米材料指南参考编号ISO/TR10993-22:2017(E)CISO2017ISO/TR10993-22:2017(E)受版权保护的文档◎ISO2017,瑞士发布版权所有。除非另有说明,未经事先书面许可,不得以任何形式或任何方式(包括电子或机械手段,如复印、发布于互联网或内联网)复制或以其他方式使用本出版物的任何部分。许可申请可向以下地址的ISO组织或请求者所在国的ISO成员机构提出。国际版权局Ch.deBlandonnet8·CP401CH-1214Ve...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
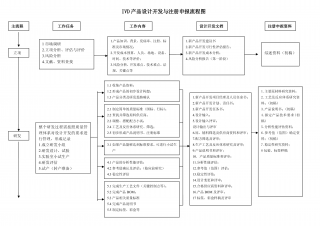
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者: 51zlzl
分类:法规规范
价格:200质量币
属性:68 页
大小:2.41MB
格式:PDF
时间:2025-11-21


