医疗器械相关法规-AUS021-受监管与不受监管软件(排除)的医疗器械示例(中文)
VIP免费
澳大利亚政府
卫生部
治疗用品管理局
受监管与不受监管软件(排除)
的医疗器械示例
版本 1.2,8月2021
健康安全条例
2D
356C 91B6D04D13155230AEF⁸
895262B127905DE65
0EAF3F5463B6EBED9DC
158948546354D3EE550
575B144F068 A6409580
3 C 04E4136C4FF07R
FF72B5Cc
TGA‘
治疗的 货物 管理
版权
a澳大利亚联邦 2021年
tga.
copyright@tga.gov.au
本作品受版权保护。您可完整或部分复制本作品且未经修改,用于个人使用;若您所属机构需内部使用,亦可复
制,但须满足以下条件:您或机构不得将复制内容用于商业用途,并在复制时保留本版权声明及所有免责声明。
除《1968年版权法》授权或本版权声明允许的使用权利外,所有其他权利均予保留。未经联邦政府书面许可,您
不得以任何形式(电子或其他方式)复制本作品的全部或部分内容。有关复制及权利的咨询,请致函澳大利亚联
邦治疗用品管理局 TGA 版权专员,地址:邮政信箱100,伍登市,澳大利亚首都领地2606;或发送电子邮件至
。
本指南旨在帮助制造商和申办方理解 TGA 如何解读相关要求,从而明确制造商和申办方应如何合
规。
本文件仅为指导性文件,建议制造商及申办方熟悉澳大利亚的立法与监管要求,并在必
要时寻求专业意见。各制造商或申办方有责任理解并遵守这些要求。
受监管与不受监管软件示例(已排除)基于软件的医疗器械 第2页,共21页
版本1.2,2021年8月
治疗用品管理局
目录
关于本指南_4
软件监管变更........... ……………………………………………………………………………………………………………………………………………………………………………………………………… 4
步行示例 _________________________________________ 5
该软件是否拟用于医疗目的?............................................................................................................ 5
该软件是否符合排除标准? -5
示例1:千焦计数器 7
例2:用于跟踪健康信息的软件_7
例3:用于诊断高血压和心脏病风险的软件 7
示例4:胰岛素泵控制软件_8
排除的软件示例_8
受监管软件示例 9
I类.................................................... 10
带状疱疹神经网络监测............................................................................................................. 10
其他I类示例................................................................................................................................10
Ila I类..................................................................................................................... 10
心脏MRI分析仪......................................................................................... 错误!书签未定义。
其他Ila类示例.............................................................................................................................10
IIb类_..................................................................................................................... 11
心脏MRI分析仪.......................................................................................................................... 11
心脏瓣膜筛查............................................................................................. 错误!书签未定义。
急性动脉闭塞的诊断..................................................................................................................11
治疗或干预建议..........................................................................................................................11
其他IIb类示例.............................................................................................................................11
III级........................................................ 12
指定治疗或干预措施................................................................................................................. 12
其他II类示例.............................................................................................................................. 12
排除 软件 与受管制的 软件.................................................................................... 12
临床决策支持软件 ................................................................. -18
受监管与不受监管软件(不包括)的医疗器械示例 第3页,共21页
2021年8月第1.2版
摘要:
展开>>
收起<<
澳大利亚政府卫生部治疗用品管理局受监管与不受监管软件(排除)的医疗器械示例版本1.2,8月2021健康安全条例2D356C91B6D04D13155230AEF⁸895262B127905DE650EAF3F5463B6EBED9DC158948546354D3EE550575B144F068A64095803C04E4136C4FF07RFF72B5CcTGA‘治疗的货物管理版权a澳大利亚联邦2021年tga.copyright@tga.gov.au本作品受版权保护。您可完整或部分复制本作品且未经修改,用于个人使用;若您所属机构需内部使用,亦可复制,但须满足以下条件:您或机构不得将复制内容用...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
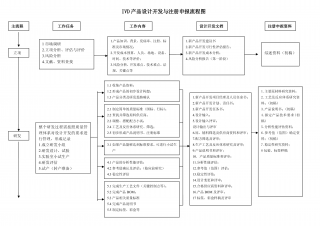
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者:冒牌货
分类:法规规范
价格:150质量币
属性:25 页
大小:1.24MB
格式:PDF
时间:2026-01-09


