IATF16949质量管理体系手册详解
标签: #IATF16949 #手册 #管理
IATF16949质量管理体系手册详解文件编号文件版本实施日期制作审核批准修订记录部门汇签部门签字部门签字序号修订日期审核批准目录章节标题识别的过程页码封面——修订记录0质量里手册优秀文档IATF16949质量管理体系手册详解目录1-7前言8颁布令9质量方针10企业概况111.管理原则112.范围与应用123.引用标准、术语和定义12-134.组织环境144.1了解组织及环境144.2了解相关方的需求和期望144.2.1了解相关方的需求和期望-补充144.3确定质量管理体系范围144.3.1确定质量管理体系范围-补充144.3.2顾客特殊要求144.4质量管理体系及其过程14-164.4.1组...
相关推荐
-
IVD产品设计开发以及注册申报流程图VIP免费
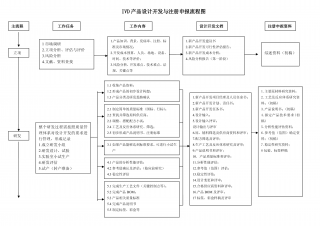
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80


