2020年全国两法知识竞赛试题及答案(715题)



摘要:
展开>>
收起<<
1、药物临床试验期间,发现存在安全性问题或者其他风险的,临床试验申办者应当向(B)报告。 A、省级药品监督管理部门 B、国务院药品监督管理部门 C、省级卫生健康主管部门 D、国务院卫生健康主管部门 2、根据药品生产监督管理相关规定,取得药品生产许可证的某企业拟改建车间,则应报经药品监督管理部门进行(A)。 A、药品生产质量管理规范符合性检查 B、药品生产质量管理规范认证检查 C、药品生产质量管理规范认证 D、飞行检查 3、因品种特性及审评、核查、检验等工作遇到特殊情况确需延长时限的,延长的时限不得超过原时限的(A)。 A、二分之一 B、三分之一 C、四分之一 D、两倍 4、药品监督管理部...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
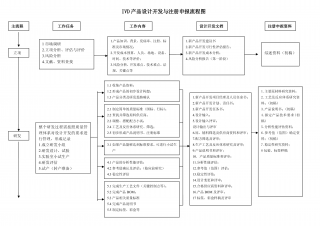
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者:宁静致远
分类:培训考试
价格:30质量币
属性:51 页
大小:90.73KB
格式:DOCX
时间:2024-05-20


