IATF16949:2016 质量手册
标签: #IATF16949 #质量手册 #手册
版本/修改码:A/0ISO9001/IATFI6949:2016质量手册CVC-QM-2017CVC-QM-2017XXXX有限公司质量手册(依据IATF16949∶2016标准编制)版本:A/0编制:审核:批准:发布日期:2017年10月11日实施日期:2017年10月11日XXXX有限公司发布目录章节及名称相关过程名称页码0.1封面 10.2目录 20.3修订登记页 71.0质量手册颁布令 81.1质量方针、质量目标颁布令 91.2公司简介 101.3任命书 111.4组织机构图 121.5各部门/岗位质量职责和权限 131.6部门职能矩阵 151.7质量管理原则 151.8过程方法简述 ...
相关推荐
-
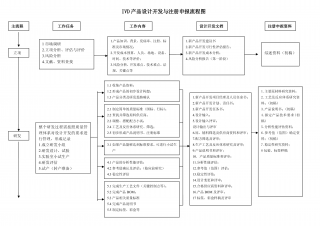
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80


