ISO 10993-11-2017 医疗器械生物学评价-第11部分全身毒性试验(中文)
VIP免费
ISO 10993-11:2017(E)中文版
国际标准
第3版
2017-09
医疗器械生物学评价—第11部分:
全身毒性试验
(中文版)
2025年07月翻译
参考版本号:
ISO 10993-11:2017(E)
PAGE:1 守道者翻译 CISO2017-Allrightsreserved
ISO 10993-11:2017(E) 中 文 版
目录
前言
.................................................................................................................................................................................................. 4
介绍 ..................................................................................................................................................................................................5
1. 范围...........................................................................................................................................................................................6
2. 规范性引用文件 .......................................................................................................................................................................
6
3. 术语及定义............................................................................................................................................................................. 6
4. 一般注意事项 ...........................................................................................................................................................................
8
4.1. 概述 .......................................................................................................................................................................................
4.2. 动物种类的选择............................................................................................................................................................. 8
4.3. 动物状态...........................................................................................................................................................................
8
4.4. 动物饲养与管理 ...............................................................................................................................................................
8
4.5. 剂量组组的大小和数量 ...................................................................................................................................................
9
4.5.1. 剂量组大小.................................................................................................................................................................
9
4.5.2. 剂量组数目...............................................................................................................................................................
9
4.5.3. 对照设置.................................................................................................................................................................. 9
4.6. 接触途径.......................................................................................................................................................................10
4.7. 样品制备 ....................................................................................................................................................................... 10
4.8. 剂量............................................................................................................................................................................... 10
4.8.1. 试验样品接触 ......................................................................................................................................................10
4.8.2. 剂量体积............................................................................................................................................................... 10
4.8.3. 剂量频率.............................................................................................................................................................. 10
4.9. 体重和饲料/水消耗.....................................................................................................................................................1
4.10. 临床观察................................................................................................................................................................... 1
4.11. 临床病理学............................................................................................................................................................... 11
4.12. 解剖病理学..................................................................................................................................................................1
4.13. 研究设计......................................................................................................................................................................12
4.14. 调查质量..................................................................................................................................................................... 12
5. 急性全身毒性...................................................................................................................................................................... 12
5.1. 概述 ............................................................................................................................................................................... 12
5.2. 研究设计 ....................................................................................................................................................................... 12
5.2.1. 准备工作 ............................................................................................................................................................... 12
5.2.2. 实验动物 ...............................................................................................................................................................13
5.2.3. 试验条件 ............................................................................................................................................................... 13
PAGE:2 守道者翻译 CISO2017-Allrightsreserved
ISO 10993-11:2017(E) 中 文 版
5.2.4. 体重....................................................................................................................................................................... 13
5.2.5. 临床观察 .............................................................................................................................................................. 13
5.2.6. 病理学.....................................................................................................................................................................14
5.3. 评价标准 ....................................................................................................................................................................... 14
5.3.1. 概述 ....................................................................................................................................................................... 14
5.3.2. 结果评价 .............................................................................................................................................................. 14
5.4. 最终报告 ....................................................................................................................................................................... 15
6. 重复接触全身毒性(亚急性、亚慢性和 慢性全身毒性)................................................................................................. 16
6.1. 概述 ............................................................................................................................................................................... 16
6.2. 研究设计 ....................................................................................................................................................................... 16
6.2.1. 准备工作...............................................................................................................................................................16
6.2.2. 实验动物............................................................................................................................................................... 16
6.2.3. 试验条件...............................................................................................................................................................17
6.2.4. 体重....................................................................................................................................................................... 17
6.2.5. 临床观察 ............................................................................................................................................................... 17
6.2.6 . 病理学..................................................................................................................................................................17
6.3. 评价标准.......................................................................................................................................................................18
6.3.1. 概述 ....................................................................................................................................................................... 18
6.3.2. 结果评估.............................................................................................................................................................. 18
6.4. 最终报告....................................................................................................................................................................... 18
附件A(资料性)接触途径 ...................................................................................................................................................... 19
附件B(资料性)剂量体积 ....................................................................................................................................................... 21
附件C(资料性)常见临床症状与观察项目................................................................................................................................. 2
附件D(资料性)建议的血液学、临床生化和尿液分析测量 ...............................................................................................23
附件E(资料性)建议进行组织病理学评价的器官清单....................................................................................................... 25
附件F(资料性)医疗器械全身毒性试验限定的组织病理学器官清单 ..............................................................................27
附件G(资料性)材料介导的热原信息.................................................................................................................................. 28
附件H(资料性)大鼠亚慢性全身毒性试验一胃 肠外双途径接角触....................................................................................... 29
参考文献
...................................................................................................................................................................................... 31
PAGE:3 守道者翻译 CISO2017-Allrightsreserved
摘要:
展开>>
收起<<
ISO10993-11:2017(E)中文版国际标准第3版2017-09医疗器械生物学评价—第11部分:全身毒性试验(中文版)2025年07月翻译参考版本号:ISO10993-11:2017(E)PAGE:1守道者翻译CISO2017-AllrightsreservedISO10993-11:2017(E)中文版目录前言..............................................................................................................................................
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
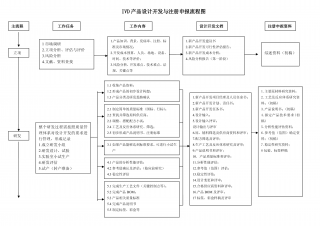
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者: 51zlzl
分类:法规规范
价格:300质量币
属性:32 页
大小:542.4KB
格式:PDF
时间:2025-11-20


