环境管理体系认证规则
VIP免费
环境管理体系认证规则
目 录
1.适用范围
2.对认证审核人员的基本要求
3.初次认证程序
4.监督审核程序
5.再认证程序
6.暂停或撤销认证证书
7.认证证书要求
8.与其他管理体系的结合审核
9.受理转换认证证书
10.受理组织的申诉
11.认证记录的管理
12.其他
附录 A 环境管理体系认证审核时间要求
1适用范围
1.1 本规则用于规范依据 GB/T 24001-2016/ISO14001:2015《环境管理体
系要求及使用指南》标准在鸿海认证开展的环境管理体系认证活动。
1.2 本规则依据认证认可相关法律法规,结合相关技术标准,对环境管理
体系认证实施过程作出具体规定,明确鸿海认证对认证过程的管理责任,保证环
境管理体系认证活动的规范有效。
1.3 本规则是鸿海认证在环境管理体系认证活动中的基本要求。
2对认证审核人员的基本要求
2.1 认证审核员应当取得国家认监委确定的认证人员注册机构颁发的环境
管理体系审核员注册资格。
2.2 认证人员应当遵守与从业相关的法律法规,对认证审核活动及相关认
证审核记录和认证审核报告的真实性承担相应的法律责任。
3初次认证程序
3.1 受理认证申请
3.1.1 鸿海认证向申请组织公开以下信息:
(1)可开展认证业务的范围,以及获得认可的情况。
(2)本规则的完整内容。
(3)认证证书样式。
(4)对认证过程的申投诉规定。
3.1.2 鸿海认证要求申请组织至少提交以下资料:
(1)认证申请书,申请书应包括申请认证的生产、经营或服务活动范围及
活动情况的说明。
(2)法律地位的证明文件的复印件。若环境管理体系覆盖多场所活动,应
附每个场所的法律地位证明文件的复印件(适用时)。
(3)环境管理体系覆盖的活动所涉及法律法规要求的行政许可证明、资质
证书、强制性认证证书等的复印件。
(4)环境管理体系覆盖的涉及环境影响的因素,国家有相应的法律法规明
确规定需办理环评报告要求的,应提供相应的资料的复印件。
(5)环境管理体系成文信息 (适用时)。
3.1.3 鸿海认证应对申请组织提交的申请资料进行评审,根据申请认证的
活动范围及场所、从事活动的环境因素影响等级、员工人数、完成审核所需时间
和其他影响认证活动的因素,综合确定是否有能力受理认证申请。
对被执法监管部门责令停业整顿或在全国企业信用信息公示系统中被列入
“严重违法企业名单”的申请组织,鸿海认证不应受理其认证申请。
3.1.4 对符合 3.1.2、3.1.3 要求的,鸿海认证可决定受理认证申请;对不
符合上述要求的,鸿海认证应通知申请组织补充和完善,或者不受理认证申请。
3.1.5 签订认证合同
在实施认证审核前,鸿海认证应与申请组织订立具有法律效力的书面认证
合同,合同应包含以下内容:
(1)申请组织获得认证后持续有效运行环境管理体系的承诺。
(2)申请组织对遵守认证认可相关法律法规,协助认证监管部门的监督检
查,对有关事项的询问和调查如实提供相关材料和信息的承诺。
(3)申请组织承诺获得认证后发生以下情况时,应及时向鸿海认证通报:
①客户及相关方有重大投诉。
②环保部门对企业的环境检查不合格。
③发生环境事故。
④相关情况发生变更,包括:法律地位、生产经营状况、组织状态或所有
权变更;取得的行政许可资格、强制性认证或其他资质证书变更;法定代表人、
最高管理者变更;生产经营或服务的工作场所变更;环境管理体系覆盖的活动范
围变更;环境管理体系和重要环境因素控制方法的重大变更等。
⑤出现影响环境管理体系运行的其他重要情况。
(4)申请组织承诺获得认证后正确使用认证证书、认证标志和有关信息,
不利用环境管理体系认证证书和相关文字、符号误导公众认为其产品或服务通过
认证。
(5)拟认证的环境管理体系覆盖的活动范围。
(6)在认证审核实施过程及认证证书有效期内,鸿海认证和申请组织各自
应当承担的责任、权利和义务。
(7)认证服务的费用、付费方式及违约条款。
摘要:
展开>>
收起<<
环境管理体系认证规则目录1.适用范围2.对认证审核人员的基本要求3.初次认证程序4.监督审核程序5.再认证程序6.暂停或撤销认证证书7.认证证书要求8.与其他管理体系的结合审核9.受理转换认证证书10.受理组织的申诉11.认证记录的管理12.其他附录A环境管理体系认证审核时间要求1适用范围1.1本规则用于规范依据GB/T24001-2016/ISO14001:2015《环境管理体系要求及使用指南》标准在鸿海认证开展的环境管理体系认证活动。1.2本规则依据认证认可相关法律法规,结合相关技术标准,对环境管理体系认证实施过程作出具体规定,明确鸿海认证对认证过程的管理责任,保证环境管理体系认证活动的规...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
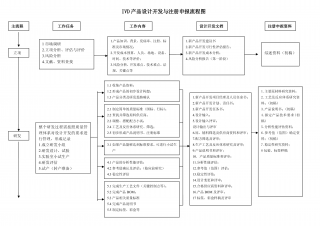
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者:多多猪
分类:实用文档
价格:60质量币
属性:15 页
大小:303.6KB
格式:PDF
时间:2025-10-27


