MDR实施医疗器材欧盟法规-20181019
VIP免费

标签: #MDR
摘要:
展开>>
收起<<
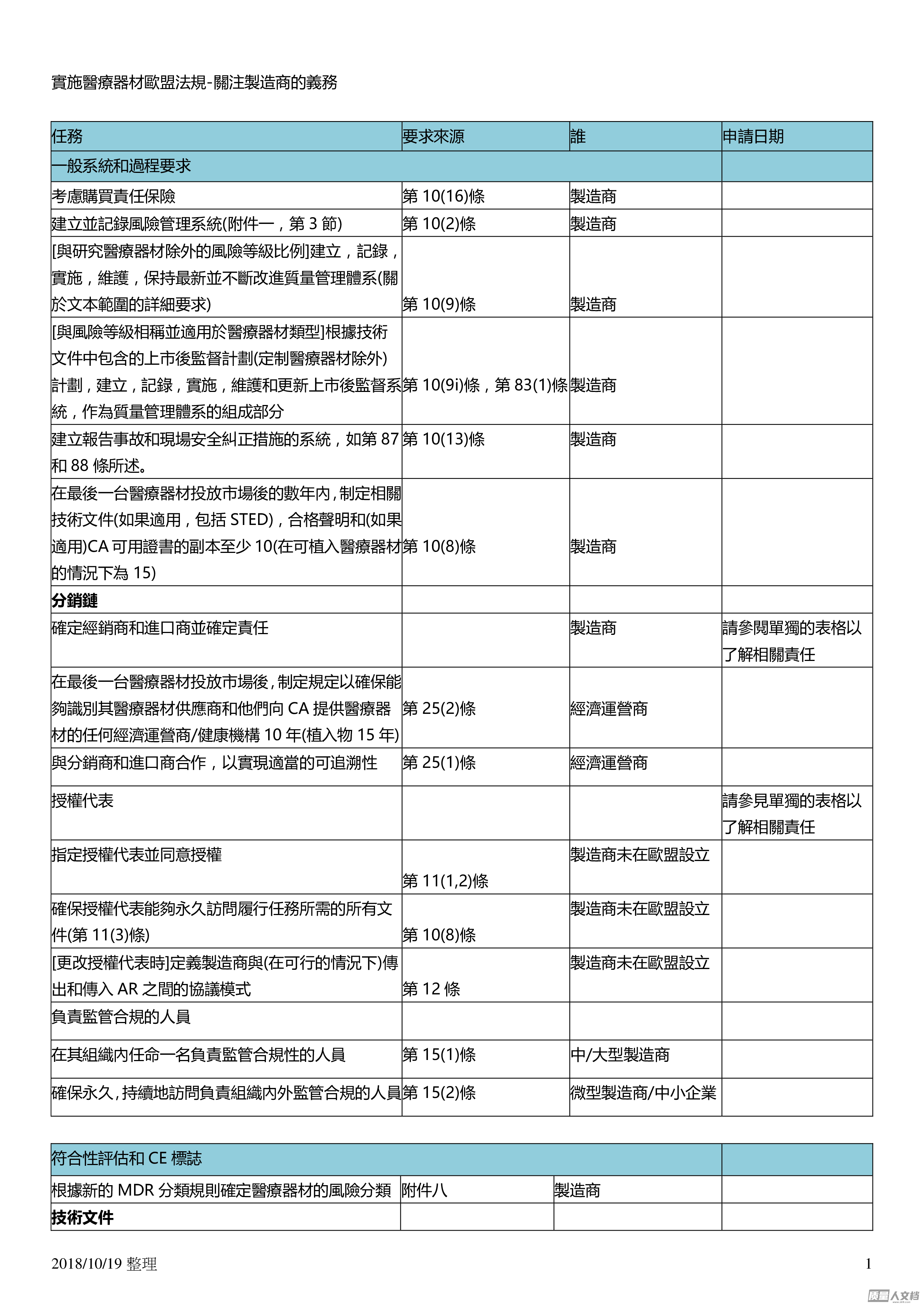
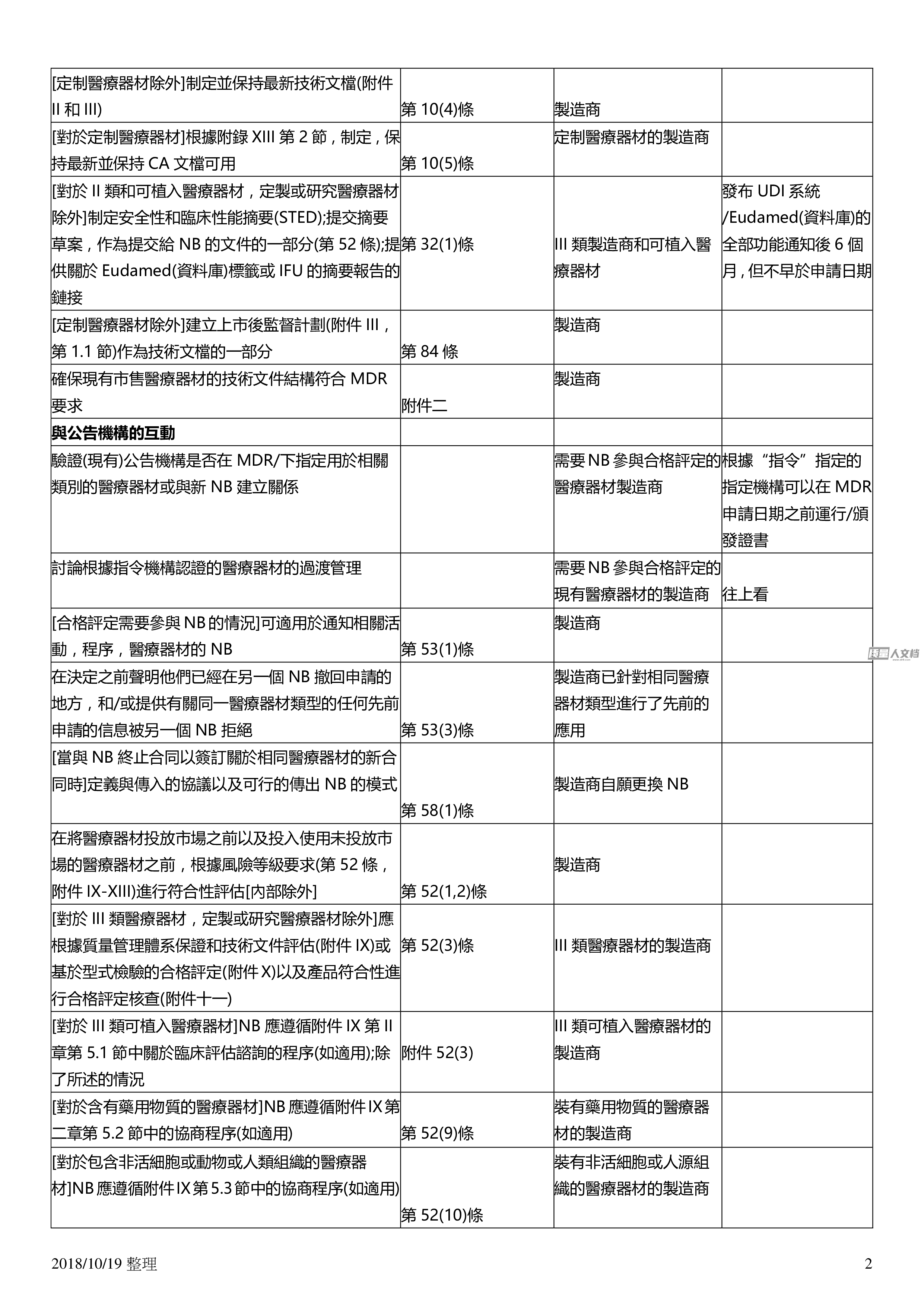
20181019整理1實施醫療器材歐盟法規關注製造商的義務任務要求來源誰申請日期一般系統和過程要求考慮購買責任保險第1016條製造商建立並記錄風險管理系統附件一第3節第102條製造商與研究醫療器材除外的風險等級比例建立記錄實施維護保持最新並不斷改進質量管理體系關於文本範圍的詳細要求第109條製造商與風險等級相稱並適用於醫療器材類型根據技術文件中包含的上市後監督計劃定制醫療器材除外計劃建立記錄實施維護和更新上市後監督系統作為質量管理體系的組成部分第109i條第831條製造商建立報告事故和現場安全糾正措施的系統如第87和88條所述。第1013條製造商在最後一台醫療器材投放市場後的數年內制定相關技術...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
纯化水中国药典2020版与2025版GAP分析VIP免费

 2025-04-18 383
2025-04-18 383 -
无菌检查法对比表(2025版药典 VS 2020版药典)

 2025-09-27 608
2025-09-27 608 -
1101无菌检查法对比表(2025版药典 VS 2020版药典)

 2025-09-29 557
2025-09-29 557 -
1143 细菌内毒素检查法对比表(2025版药典 VS 2020版药典)

 2025-09-29 999+
2025-09-29 999+ -
TR-26-2025-Sterilizing-Filtration-of-Liquids液体的灭菌过滤(中英文对照版)VIP专享

 2025-11-06 520
2025-11-06 520 -
TR-26-2025-Sterilizing-Filtration-of-Liquids液体的灭菌过滤(英文版)VIP免费

 2025-11-06 176
2025-11-06 176 -
PDA-TR49-生物清洁验证-中英文翻译

 2025-11-19 186
2025-11-19 186 -
注射用药品的目视检查-第五版-2025.10_中文VIP免费

 2025-11-25 82
2025-11-25 82 -
硫酸艾玛昔替尼片(CXHS2300097)说明书VIP免费

 2025-11-26 438
2025-11-26 438 -
PDA TR60 Process Validation A Lifecycle Approach 2026VIP免费

 2026-03-19 85
2026-03-19 85
作者:胖子
分类:法规规范
价格:30质量币
属性:11 页
大小:469.89KB
格式:PDF
时间:2024-05-13


