《北京市医疗器械审评核查咨询问答 300 问》-下册



标签: #医疗器械
摘要:
展开>>
收起<<
《北京市医疗器械审评核查咨询问答300问》(下册)发布时间:2023年07月05日第一篇有源产品201.第二类独立软件产品删减部分非核心临床功能是否需要补检?答:如果删减部分非核心临床功能不影响医疗器械安全性与有效性,这种情况属于轻微软件更新,一般不需要补检。如果删减部分非核心临床功能影响医疗器械安全性与有效性,则属于重大软件更新,这种情况一般需要进行补检。202.第二类有源产品的研发过程中何时需要进行联合使用的研究?答:如申报产品预期与其他医疗器械、药品、非医疗器械产品联合使用实现同一预期用途,应提供证明联合使用安全有效的研究资料,包括互联基本信息(连接类型、接口、协议、最低性能)、联合使用...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
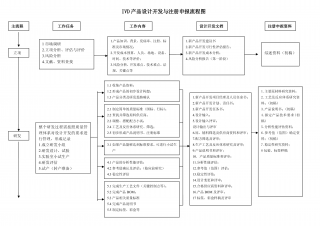
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 260
2024-04-12 260 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 345
2024-04-12 345 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 349
2024-04-12 349 -
创新医疗器械注册申报流程

 2024-05-02 176
2024-05-02 176 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 128
2024-05-09 128 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 351
2024-11-18 351 -
内审检查表 MDR法规VIP免费

 2025-04-07 323
2025-04-07 323 -
07.产品风险管理报告VIP免费

 2025-09-12 88
2025-09-12 88 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 130
2025-09-12 130 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 80
2025-11-03 80
作者:胖子
分类:专业资料
价格:免费
属性:24 页
大小:438.24KB
格式:PDF
时间:2024-09-08


