医疗器械注册质量体系核查的程序和检查


摘要:
展开>>
收起<<
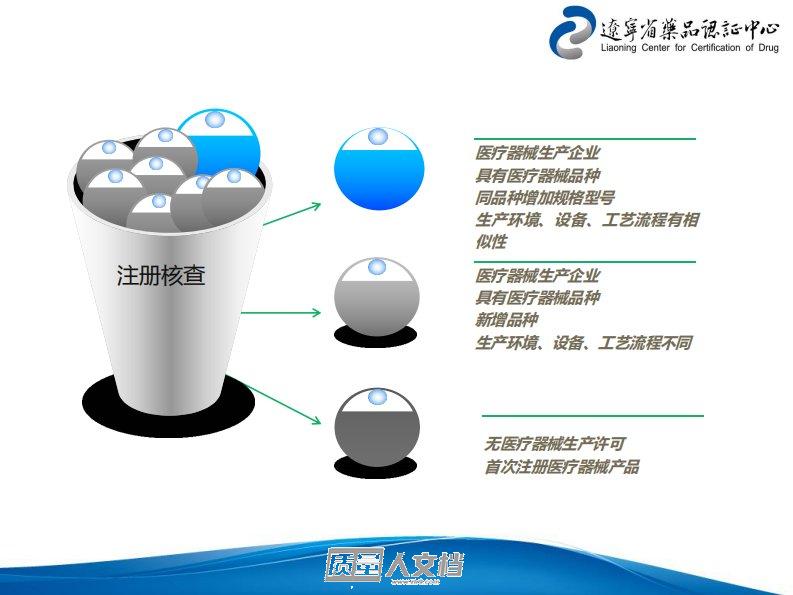
辽宁省医疗器械注册质量体系核查检查要求目的1.判断研制和样品生产过程是否按规范进行2.是否在体系内受控3.判断研制过程是否真实4.判断样品是否真实生产5.判断企业是否具备生产能力(厂房、设施设备、工艺、SOP)6.申报资料关键内容是否与设计输出一致医疗器械生产企业具有医疗器械品种同品种增加规格型号生产环境、设备、工艺流程有相似性医疗器械生产企业具有医疗器械品种新增品种生产环境、设备、工艺流程不同无医疗器械生产许可首次注册医疗器械产品注册核查1•62家企业•101个品种•331条缺陷项(48条主要缺陷)注册核查主要存在的问题17.2.1应当编制生产工艺规程、作业指导书等,明确关键工序和特殊过程。...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
纯化水中国药典2020版与2025版GAP分析VIP免费

 2025-04-18 375
2025-04-18 375 -
无菌检查法对比表(2025版药典 VS 2020版药典)

 2025-09-27 579
2025-09-27 579 -
1101无菌检查法对比表(2025版药典 VS 2020版药典)

 2025-09-29 488
2025-09-29 488 -
1143 细菌内毒素检查法对比表(2025版药典 VS 2020版药典)

 2025-09-29 968
2025-09-29 968 -
ECA-污染控制策略指南(中英文)-202202VIP免费

 2025-11-04 95
2025-11-04 95 -
TR-26-2025-Sterilizing-Filtration-of-Liquids液体的灭菌过滤(中英文对照版)VIP专享

 2025-11-06 506
2025-11-06 506 -
TR-26-2025-Sterilizing-Filtration-of-Liquids液体的灭菌过滤(英文版)VIP免费

 2025-11-06 168
2025-11-06 168 -
PDA-TR49-生物清洁验证-中英文翻译

 2025-11-19 162
2025-11-19 162 -
硫酸艾玛昔替尼片(CXHS2300097)说明书VIP免费

 2025-11-26 413
2025-11-26 413 -
PDA TR60 Process Validation A Lifecycle Approach 2026VIP免费

 2026-03-19 77
2026-03-19 77
作者:宁静致远
分类:培训考试
价格:50质量币
属性:30 页
大小:783.79KB
格式:PDF
时间:2024-05-20


